Avaliação automática da qualidade do sinal
Ao trabalhar com dados de fNIRS, obter sinais de alta qualidade é essencial para garantir resultados confiáveis. Nosso Support Hub oferece dicas práticas para ajudar você a otimizar a aquisição dos sinais. No entanto, mesmo seguindo as melhores práticas, desafios como cabelos escuros ou espessos e tecido do couro cabeludo altamente pigmentado podem levar a uma baixa qualidade do sinal em alguns canais.
Isso é particularmente relevante para sistemas de alta densidade, como o Brite ou o MultiBrite, em que o grande número de optodos torna difícil garantir boa qualidade em todos os canais. Avaliar manualmente a qualidade dos sinais se torna inviável, especialmente em conjuntos de dados extensos.
As métricas automáticas de qualidade de sinal oferecem uma solução eficiente. Neste post, explicamos o que significa ter boa qualidade de sinal em fNIRS, apresentamos diferentes métodos de avaliação automática da qualidade do sinal fNIRS e listamos suas vantagens e desvantagens.
O que é uma boa qualidade de sinal em fNIRS?
Além da resposta hemodinâmica evocada pela tarefa, o sinal de fNIRS também contém ritmos fisiológicos, como frequência cardíaca e respiração. Embora esses componentes sejam frequentemente considerados ruído durante análises cognitivas, eles podem ser aproveitados em análises avançadas, como a extração da frequência cardíaca ou respiratória (veja nossos posts sobre frequência cardíaca e frequência respiratória).
A presença de um ciclo cardíaco nítido, especialmente no sinal de hemoglobina oxigenada (O2Hb) (veja a Figura 1), é um forte indicador de boa acoplagem entre o optodo e o couro cabeludo. Em outras palavras, se os batimentos cardíacos são claramente visíveis, o sinal é considerado de boa qualidade.
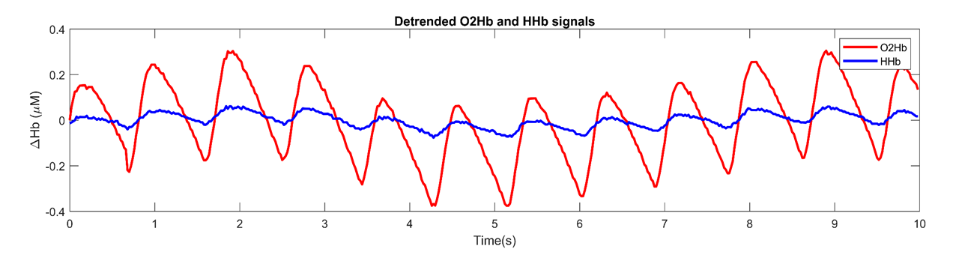
Figura 1: Segmento de uma medição de fNIRS. Em vermelho, a hemoglobina oxigenada (O2Hb); em azul, a hemoglobina desoxigenada (HHb).
Algoritmos de qualidade de sinal
Diversos algoritmos foram desenvolvidos para automatizar a avaliação da qualidade do sinal. A seguir, apresentamos quatro abordagens comumente utilizadas.
Coeficiente de Variação (CV)
Um dos métodos é o Coeficiente de Variação (CV), uma medida estatística de variabilidade relativa frequentemente aplicada aos sinais de intensidade luminosa bruta [1]:
CV = (Desvio Padrão / Média) * 100%
Um CV alto geralmente indica um sinal instável, o que pode resultar de movimentos, má qualidade de contato dos optodos ou ruído sistêmico.
Vantagem (PRO): o CV é uma solução simples e direta para automatizar a avaliação da qualidade do sinal.
Desvantagem (CON): a principal limitação do CV é que ele não diferencia flutuações fisiológicas (como batimentos cardíacos ou respiração) de artefatos de movimento. Isso pode levar à rejeição incorreta de sinais bons ou à aceitação de sinais ruins com pouca variação.
Por isso, é necessário ajustar cuidadosamente os limiares para cada caso. Além disso, recomenda-se verificar visualmente os segmentos de dados para identificar sinais planos e evitar falsos negativos.
Índice de Acoplamento ao Couro Cabeludo (SCI – Scalp Coupling Index)
O SCI foi desenvolvido para avaliar o contato entre optodo e couro cabeludo com base na presença de oscilações cardíacas no sinal bruto [2]. Ele calcula a correlação entre dois comprimentos de onda (geralmente 760 e 850 nm).
Vantagem (PRO): a ideia é simples — sinais fisiológicos afetam ambos os comprimentos de onda de forma semelhante, enquanto ruído aleatório ou mau contato não. Assim, alta correlação indica boa qualidade de sinal, e baixa correlação indica má qualidade.
Desvantagem (CON): o principal problema é que ruídos que afetam igualmente ambos os comprimentos de onda, como artefatos de movimento, podem gerar alta correlação e, portanto, passar despercebidos.
Na literatura, valores de SCI ≥ +0,75 ou +0,80 são frequentemente usados para classificar canais como bons e aceitáveis para análise [2, 3].
PHOEBE – Placing Headgear Optodes Efficiently Before Experimentation
O PHOEBE foi desenvolvido para superar as limitações do SCI, combinando-o com análise espectral [4].
Ele examina a potência espectral da correlação cruzada entre comprimentos de onda, focando especificamente na intensidade do pico cardíaco.
Sinais de boa qualidade apresentam um pico dominante e bem definido na frequência cardíaca, enquanto sinais com artefatos de movimento mostram espectros mais amplos e difusos, com menor potência de pico.
Vantagem (PRO): ao isolar o componente cardíaco, o PHOEBE melhora a sensibilidade para detectar canais de baixa qualidade, mesmo na presença de movimento.
Índice de Qualidade do Sinal (SQI – Signal Quality Index)
Como um método mais detalhado e robusto para avaliar a qualidade do sinal fNIRS, foi desenvolvido o Índice de Qualidade do Sinal (SQI) [5].
Diferentemente das abordagens anteriores, que apenas classificam os canais como “bons” ou “ruins”, o SQI fornece uma escala numérica de 1 a 5, permitindo avaliações mais flexíveis e informativas.
Vantagem (PRO): o algoritmo foca na detecção do componente cardíaco no sinal, um forte indicador de boa acoplagem optodo-couro cabeludo. Ele combina diversas etapas de processamento em três fases sequenciais de classificação:
-
Identificação de sinais de qualidade muito baixa
-
Identificação de sinais de qualidade muito alta
-
Avaliação final da qualidade do sinal
A combinação dessas etapas em um algoritmo sofisticado garante desempenho superior do SQI em comparação com o SCI e o PHOEBE [5]. Mais informações podem ser encontradas neste artigo.